距離一月賽季僅(jin) 有五周時間,目前各科目已陸續進入複習(xi) 篩查的階段,對於(yu) 各模塊知識點全麵多維的鞏固強化是現下的重中之重。化學 U4是 A2階段的關(guan) 鍵銜接,與(yu) 前期積累的基礎內(nei) 容相承接,同時在難度和綜合性上都有所提升,也是最終合分前的關(guan) 鍵一役。本篇將由理綜教研部老師結合教材核心考點,為(wei) 大家整合回顧化學 U4中那些不容失分的要點內(nei) 容。
模塊側(ce) 重
要點整合
『化學動力學』
作為(wei) 化學 U4的第一模塊,化學動力學 (Kinetics)融合了 U2模塊的反應速率,並在此基礎上加入了反應機理 (Mechanism),需明確 rate determining step類似木桶理論中的“短板原則”,即反應中最慢的步驟,決(jue) 定反應的整體(ti) 進度。這一步驟中參與(yu) 反應的物質個(ge) 數將直接決(jue) 定反應機理是屬於(yu) SN1還是 SN2,這也是貫穿 U4的關(guan) 鍵知識點之一。
而 half-life,反應物濃度減至一半所需的時間,則是判定反應級數 (Order of Reaction)的依據之一,即 half-life隨著反應進行保持恒定則反應中該反應物屬於(yu) first order with respect to the reactant;而 half-life隨著反應進行在翻倍,則反應中該反應物對應second order with respect to the reactant;當反應物濃度與(yu) 時間的坐標圖呈直線下降趨勢斜率不變時,則反應中該反應物對應 zero order with respect to the reactant。
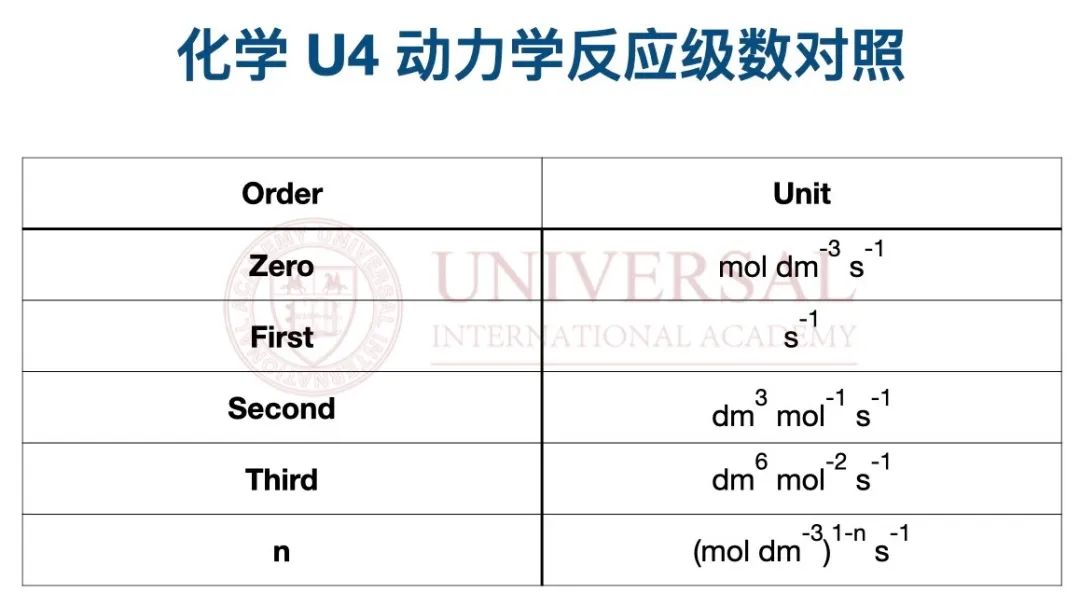 來源:理綜教研部化學 U4動力學講義(yi) 截圖
來源:理綜教研部化學 U4動力學講義(yi) 截圖
另外結合書(shu) 中整理反應的級數對應速率常數 rate constant的單位,這是部分考生容易遺漏和出錯的一環,理綜教研部歸納單位檢驗時可代入對應公式 ,其中 n則是反應的級數,而單位確認不僅(jin) 是這一單元的專(zhuan) 屬,包括後麵章節中的各類運算,單位的檢查都是必不可少的環節之一,還需引起重視。而作圖部分同樣是這一單元中容易混淆的一塊內(nei) 容,除了最基礎的濃度與(yu) 時間坐標圖,還有 1/t與(yu) 濃度坐標圖 (t為(wei) 時間),以及lnk與(yu) 1/T坐標圖 (T為(wei) 溫度),尤其是後兩(liang) 者的橫縱軸標注一定注意區分。
,其中 n則是反應的級數,而單位確認不僅(jin) 是這一單元的專(zhuan) 屬,包括後麵章節中的各類運算,單位的檢查都是必不可少的環節之一,還需引起重視。而作圖部分同樣是這一單元中容易混淆的一塊內(nei) 容,除了最基礎的濃度與(yu) 時間坐標圖,還有 1/t與(yu) 濃度坐標圖 (t為(wei) 時間),以及lnk與(yu) 1/T坐標圖 (T為(wei) 溫度),尤其是後兩(liang) 者的橫縱軸標注一定注意區分。
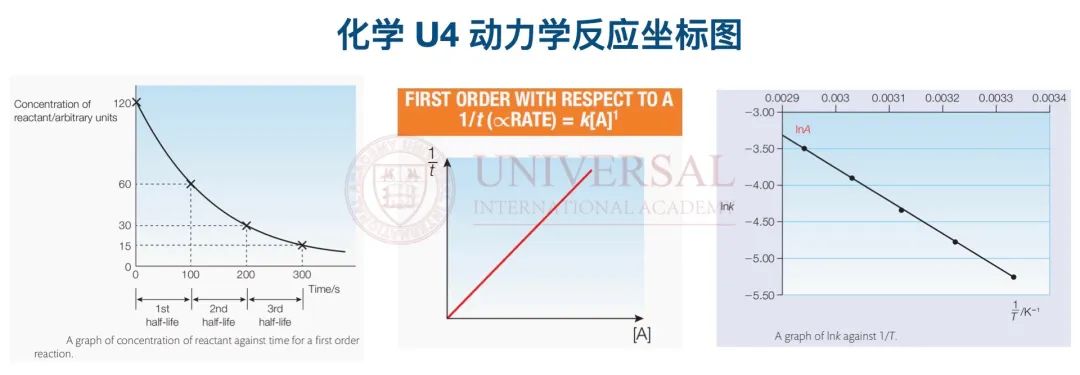 來源:理綜教研部化學 U4動力學講義(yi) 截圖
來源:理綜教研部化學 U4動力學講義(yi) 截圖
『熵變與(yu) 能量學』
這一章節是對反應是否自發進行的討論,而這需要同時滿足 Thermodynamic Stability和 Kinetic Stability兩(liang) 方麵均處於(yu) unstable狀態,分別對應總熵 Total Entropy為(wei) 正值以及活化能 Activation Energy較低。也就是說,將 Entropy Change of the System與(yu) Entropy Change of the Surroundings相加得到的 Total Entropy若為(wei) 正值,則反應為(wei) Thermodynamically Unstable,滿足自發反應的條件之一;而若 Activation Energy較低,則反應為(wei) Kinetically Unstable,滿足自發反應的條件之二。兩(liang) 者同時滿足,Spontaneous Reaction得以形成。
此處尤其注意 Entropy Change of the Surroundings的公式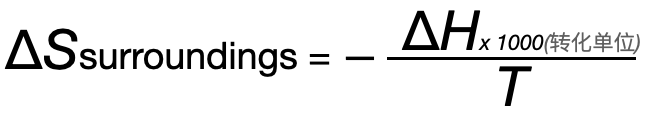 ,可知其正負與(yu) Enthalpy Change of Reaction相反,在討論 Total Entropy的正負時,若 Entropy Change of the System與(yu) Entropy Change of the Surroundings正負相反,則需將兩(liang) 者數值的 magnitude進行比較,得出最終的 Thermodynamic Stability。
,可知其正負與(yu) Enthalpy Change of Reaction相反,在討論 Total Entropy的正負時,若 Entropy Change of the System與(yu) Entropy Change of the Surroundings正負相反,則需將兩(liang) 者數值的 magnitude進行比較,得出最終的 Thermodynamic Stability。
 來源:理綜教研部化學 U4能量學講義(yi) 截圖
來源:理綜教研部化學 U4能量學講義(yi) 截圖
另外涉及內(nei) 容較為(wei) 細碎的部分即是需要考慮完整能量轉化的 Born-Haber Cycle與(yu) Hess's Law的進一步應用。除了之前單元中已接觸過的 Standard Enthalpy Change of Atomisation、Ionisation Energy與(yu) Standard Enthalpy Change of Formation之外,構成完整的 Born-Haber Cycle還需加入 Electron Affinity和 Standard Lattice Energy。理綜教研部溫馨提示 Atomisation應發生在 Ionisation和 Electron Affinity之前,注意回歸定義(yi) 和方程式。
『化學平衡』
平衡在理論層麵可以說是與(yu) U2第九單元並無出入,隻是加入了數據運算的板塊。不過需要明確的是,Kp運算自然隻涉及氣體(ti) 數據,而在 homogenous reaction中Kc運算時的數據也隻來自統一狀態的物質,heterogeneous目前階段同樣不考慮組合狀態的表達式。此處數值運算和單位的判定同樣是部分考生容易出現錯漏的部分,還需回歸教材例題,注意清晰梳理。
由於(yu) 運算環節相較而言會(hui) 更具綜合性,此處將重點展開 Kp的運算細節。首先對於(yu) 摩爾數的推算同樣滿足按照係數運算反應和生成的量,不過需注意最終代入 Kp運算公式的是平衡時各物質的 Partial Pressure,則需考慮各物質在平衡時的摩爾占比與(yu) 總氣壓的乘積。
 來源:理綜教研部模擬作答過程圖
來源:理綜教研部模擬作答過程圖
以上理綜教研部模擬作答中該考生在運算過程中出現了反應物係數錯漏的問題,即需注意反應物消耗和生成物產(chan) 生的量都是以係數作為(wei) 比例進行增減的,這直接影響到平衡時各物質的對應占比。本身並不是困難點,主要還是在運算邏輯上需要清晰把握,不遺漏細節。
另外在表述部分引入了 Qc和 Qp的概念,也就對應了平衡模塊的數據表述,注意 Kc和 Kp僅(jin) 隨溫度發生改變,不過 Qc和 Qp為(wei) 瞬間值,即改變反應物或生成物數據的那一刻的反應商,雖算法上與(yu) Kc和 Kp一致,不過數值會(hui) 有所偏移,這也正是在表述環節需要加入內(nei) 容。理綜教研部溫馨提示當反應物或生成物數據變化時,運算 Qc或 Qp時需注意總體(ti) 積或總摩爾數的調整,反應平衡向 Kc和 Kp的方向進行,以回歸恒定的平衡常數。
『酸堿平衡』
章節開篇進一步定義(yi) 了酸和堿,即 proton donor為(wei) 酸,proton acceptor為(wei) 堿,這也是酸堿專(zhuan) 題中相當關(guan) 鍵的理論基礎,可直接遞推 conjugate acid-base pair。而由於(yu) 公式相對較多,計算部分同樣是該模塊十分容易混淆的部分。以下列出專(zhuan) 題所需公式,還需注意各自對應的使用場景。
 來源:理綜教研部化學 U4酸堿講義(yi) 截圖
來源:理綜教研部化學 U4酸堿講義(yi) 截圖
除弱酸和弱堿滴定時僅(jin) 出現 point of inflection,無法使用指示劑確認 equivalence point外,其它情況下酸堿滴定時都會(hui) 出現一定長度的 steep section,也就對應了指示劑的選擇,需將指示劑的 pH range與(yu) 滴定實驗中的 steep section相重合,即可通過指示劑顏色變化的 end point確認 equivalence point。
而 Buffer Solution同樣是酸堿專(zhuan) 題中的必考內(nei) 容之一,運算部分需要考慮:在 half-equivalence point時,酸與(yu) 其共軛堿的濃度一致,此時溶液的 pH值與(yu) pKa相等。另外在計算 pH值時,若酸性溶液中的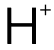 濃度低於(yu) 該溫度下水電離的
濃度低於(yu) 該溫度下水電離的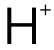 濃度,則按中性判定 pH值;堿性溶液中
濃度,則按中性判定 pH值;堿性溶液中  濃度低於(yu) 該溫度下水電離的
濃度低於(yu) 該溫度下水電離的 濃度,同樣按中性判定 pH值。例:298K,酸性溶液中
濃度,同樣按中性判定 pH值。例:298K,酸性溶液中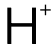 濃度低於(yu)
濃度低於(yu)  ,則判定其 pH值為(wei) 7。
,則判定其 pH值為(wei) 7。
『有機化學:羰基、羧酸與(yu) 手性』
這一章節涉及物質檢驗以及實驗現象表述較多,包括 aldehyde的四種檢驗方式、nitrile和 ester分別對應的兩(liang) 種水解方式、以及 carbonyl compound的檢驗與(yu) iodoform reaction的實驗,都是部分考生比較容易混淆的內(nei) 容,而理綜教研部強調理解記憶,以下列出部分本專(zhuan) 題涉及的部分物質檢驗,還需回歸原理,尤其清晰把握具體(ti) 官能團發生的實際反應規律,避免機械背記而導致的錯漏和失分。
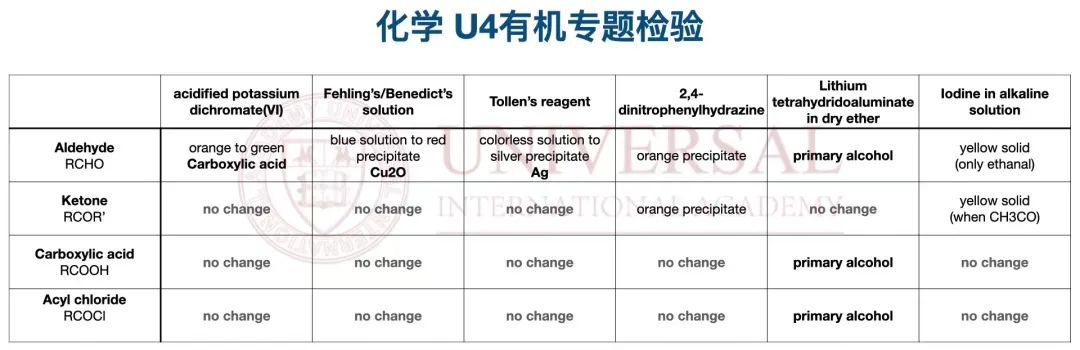 來源:理綜教研部化學 U4有機檢驗講義(yi) 截圖
來源:理綜教研部化學 U4有機檢驗講義(yi) 截圖
對於(yu) Chromatography,應注意區分幾類分離方法的構成與(yu) 優(you) 缺差異,尤其把握 stationary phase與(yu) mobiles phase分別指代的物質對象,這將直接影響分離過程中各成分最終的 retention time,即物質受 mobiles phase吸引越大,也就是受 stationary phase吸引越小,則 retention time越短。而 Chromatography常與(yu) Mass Spectrometer聯合應用以精準判定物質成分與(yu) 結構,前者給出大致的物質數據,後者則是通過 molecular ion peak以及 fragmentation peak做出精確匹配。
NMR與(yu) 圖像中的 splitting pattern是部分考生會(hui) 比較頭疼的內(nei) 容,尤其需理解相鄰原子的互相影響,清晰梳理才是關(guan) 鍵。其中大部分有機物進入 NMR係統時需溶於(yu)  ,因為(wei) 其
,因為(wei) 其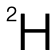 含偶數個(ge) nucleon number,核子旋轉方向相互抵消,不會(hui) 在 NMR中產(chan) 生幹擾。而 TMS(tetramethylsilane)含有完全對稱的結構,同時所含有的 12個(ge) H均屬同一化學環境,則被認為(wei) 是橫軸 chemical shift作為(wei) 對照的 0ppm。
含偶數個(ge) nucleon number,核子旋轉方向相互抵消,不會(hui) 在 NMR中產(chan) 生幹擾。而 TMS(tetramethylsilane)含有完全對稱的結構,同時所含有的 12個(ge) H均屬同一化學環境,則被認為(wei) 是橫軸 chemical shift作為(wei) 對照的 0ppm。
 來源:理綜教研部化學 U4有機核磁共振講義(yi) 截圖
來源:理綜教研部化學 U4有機核磁共振講義(yi) 截圖
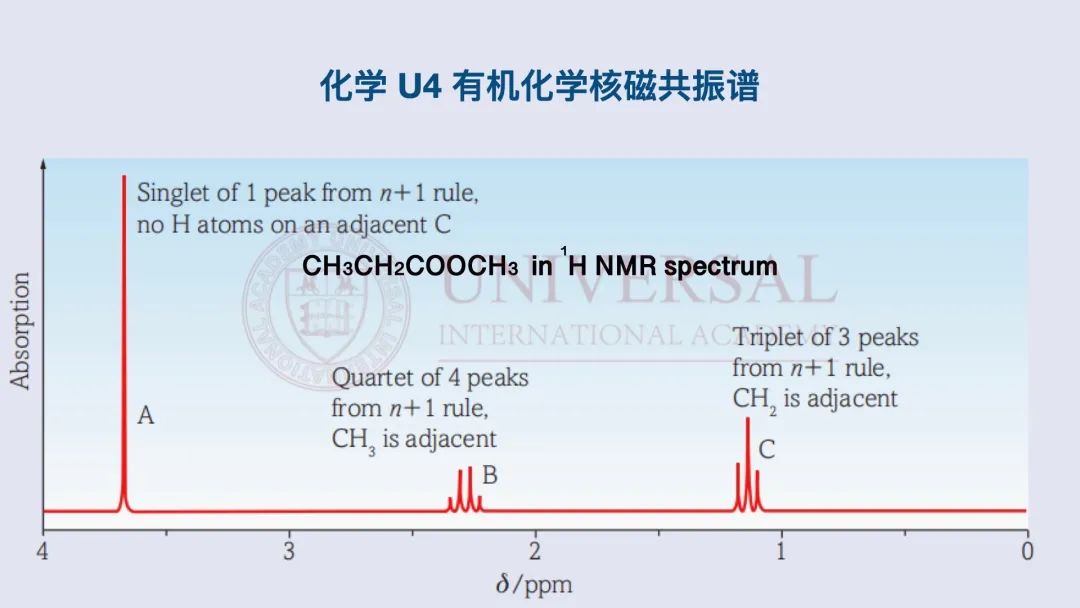
由於(yu) 不同的化學環境會(hui) 對相鄰的碳原子造成影響,則若該碳原子連有 n個(ge) 氫原子,則與(yu) 其相鄰的碳原子在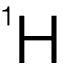 NMR中將會(hui) 顯示 n+1個(ge) sub-peak,例:
NMR中將會(hui) 顯示 n+1個(ge) sub-peak,例: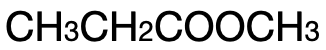 自左往右在 High Resolution Spectrum中依次產(chan) 生 3、4、1個(ge) sub-peak。其中左起第一個(ge) 碳原子右側(ce) 碳原子連有 2個(ge) 氫原子,則產(chan) 生 3個(ge) sub-peak,稱為(wei) triplet;而左起第二個(ge) 碳的左側(ce) 碳原子共連有 3個(ge) 氫原子,因此產(chan) 生 4個(ge) sub-peak,稱為(wei) quartet;最右側(ce) 碳原子相鄰原子並非碳且無氫原子相連,則產(chan) 生 1個(ge) peak,稱為(wei) singlet。這塊內(nei) 容尤其注意對象指代,切不可模棱兩(liang) 可,具體(ti) chemical shift參照公式書(shu) 與(yu) 橫軸做垂線進行範圍對應即可。
自左往右在 High Resolution Spectrum中依次產(chan) 生 3、4、1個(ge) sub-peak。其中左起第一個(ge) 碳原子右側(ce) 碳原子連有 2個(ge) 氫原子,則產(chan) 生 3個(ge) sub-peak,稱為(wei) triplet;而左起第二個(ge) 碳的左側(ce) 碳原子共連有 3個(ge) 氫原子,因此產(chan) 生 4個(ge) sub-peak,稱為(wei) quartet;最右側(ce) 碳原子相鄰原子並非碳且無氫原子相連,則產(chan) 生 1個(ge) peak,稱為(wei) singlet。這塊內(nei) 容尤其注意對象指代,切不可模棱兩(liang) 可,具體(ti) chemical shift參照公式書(shu) 與(yu) 橫軸做垂線進行範圍對應即可。
以上就是理綜教研部針對化學 U4中各模塊要點內(nei) 容的梳理歸納,還需反複閱讀,理解內(nei) 化,預祝各位在即將開啟的一月賽季中能夠做到理想發揮,順利攻克每一道關(guan) 卡!













評論已經被關(guan) 閉。