有機化學中的親(qin) 核取代反應機理
Organic Chemistry:Nucleophilic Substitution Mechanism
以鹵代烷烴halogenoalkanes為(wei) 例:
✅ 實驗1:溴甲烷與(yu) 堿水溶液發生水解取代反應時,反應速率與(yu) 溴甲烷和堿兩(liang) 者的濃度都成正比。
✅ 實驗2:叔丁基溴與(yu) 極性溶劑(如水H2O)發生取代反應時,反應速率卻僅(jin) 與(yu) 叔丁基溴的濃度成正比。
01、這是為(wei) 什麽(me) 呢?
這與(yu) 反應速率控製步驟(速控步)相關(guan) 。關(guan) 於(yu) 飽和碳原子上的親(qin) 核取代反應,通常有兩(liang) 種反應機理:雙分子親(qin) 核取代反應機理(TheSN2 Mechanism)和單分子親(qin) 核取代反應機理(The SN1 Mechanism)
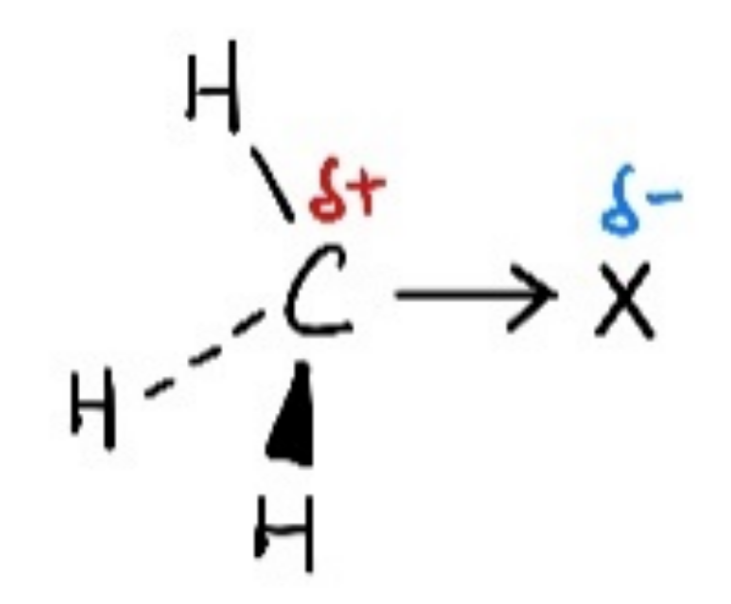
The halogen is more electronegative than carbon. Sothe carbon-halogen bond is polarized.
02、實驗1
對於(yu) 溴甲烷這個(ge)
伯鹵代烷(primary halogenoalkanes),當離去基團溴原子離開中心碳原子的同時,親(qin) 核試劑OH-也與(yu) 中心碳原子發生了部分的鍵合。
因此鍵的斷裂與(yu) 鍵的形成同時發生,中間有一個(ge) 過渡態,體(ti) 係能量達到最高。
整個(ge) 反應過程一步完成,反應速率與(yu) 溴甲烷和堿兩(liang) 者的濃度都成正比,即雙分子親(qin) 核取代反應機理(TheSN2 Mechanism)。

立體(ti) 化學特征:
發生雙分子親(qin) 核取代時,親(qin) 核試劑是從(cong) 離去基團的背麵進攻中心碳原子,原因是此方向進攻受離去基團的電子效應和空間效應的影響最小,需要的能量最低,最易發生。
因此,對於(yu) 中心碳原子是手性碳原子的情況,構型會(hui) 發生反轉,即Walden轉化。
03、實驗2
對於(yu) 叔丁基溴這個(ge)
叔鹵代烷(tertiaryhalogenoalkanes),反應分三步進行:
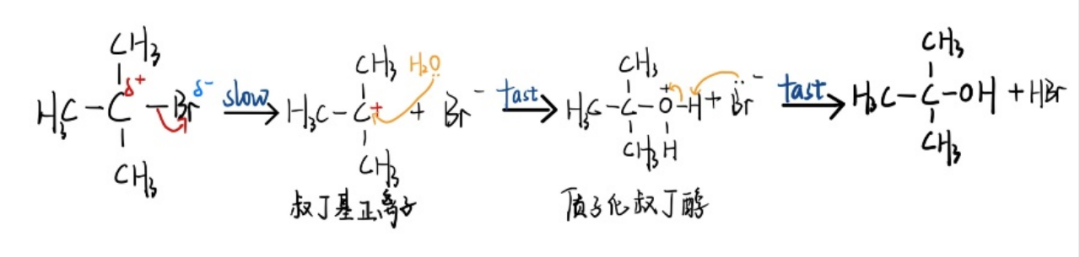
✅ 第一步,叔丁基溴在溶劑中成鍵電子對偏向溴原子後解離生成溴離子和叔丁基正離子(能量較高的活性中間體(ti) ),反應所需能量高故速度慢即為(wei) 決(jue) 定該反應速率的速控步。
✅第二步,叔丁基正離子與(yu) 水H2O親(qin) 核試劑快速結合,生成質子化叔丁醇。
✅第三步,質子化叔丁醇快速將質子轉移,獲得產(chan) 物。此過程速控步反應速率僅(jin) 與(yu) 叔丁基溴相關(guan) ,即單分子親(qin) 核取代反應機理(The SN1 Mechanism)。
立體(ti) 化學特征:
發生單分子親(qin) 核取代時,由於(yu) 反應的活性中間體(ti) 為(wei) 碳正離子,中心碳原子平麵構型為(wei) sp2雜化。親(qin) 核試劑與(yu) 之反應時,可從(cong) 平麵的兩(liang) 側(ce) 進攻中心碳原子。
因此,對於(yu) 中心碳原子是手性碳原子的情況,所得產(chan) 物是由兩(liang) 種構型相反的化合物組成的外消旋混合物。碳正離子還常常伴隨著重排反應的產(chan) 生。
一般來說,
仲鹵代烷烴(secondary halogenoalkanes)兩(liang) 種機製都可能發生,取決(jue) 於(yu) 實際的鹵代烴和反應條件。並且,大多數親(qin) 核取代反應往往介於(yu) 兩(liang) 種反應之間,並沒有絕對的SN2 反應和SN1 反應,外消旋化的同時也伴隨著構型反轉。














評論已經被關(guan) 閉。